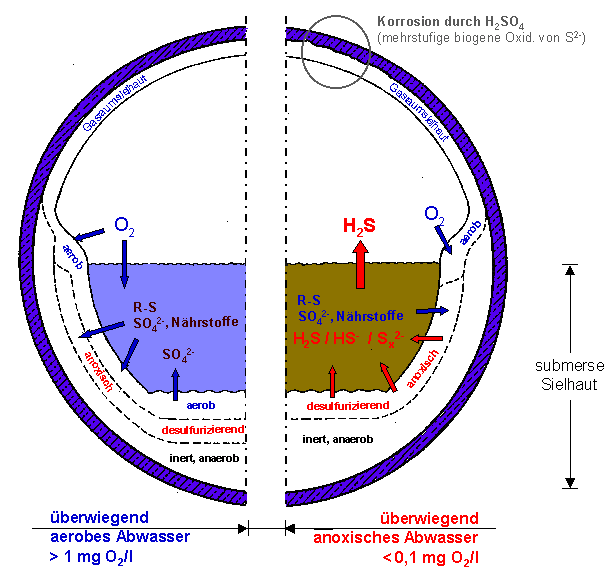
Durch Korrosion werden hauptsächlich Kanalbauwerke aus Beton und die vorhandenden Metallgeräte stark geschädigt.
Schwefelwasserstoff ist ein in Wasser lösliches Gas. Biogas und Abwasserkanäle enthalten immer eine gewisse Menge Wasserdampf.
Kondensiert dieser Dampf an kalten Stellen in der Biogasanlage oder im Abwasserkanal, so löst sich darin auch das H2S und bildet mit dem Wasser eine sehr saure und korrosive wirkende Lösung. Diese Säure korrodiert alle metallischen Bauteile (z.B. Rohrleitungen) oder greift den Beton an und zerstören diesen.
|
(1) |
H2S + H2O |
——► |
H3O+ + HS - |
Diese wässrige Lösung reagiert sauer.
Auch nachlesbar unter: Bericht des Werkstoffausschusses des Vereins Deutscher Eisenhüttenleute. Nr. 1543.
Untersuchungen über die Schädigung von Stählen unter Einfluss von feuchtem Schwefelwasserstoff
von Verein Deutscher Eisenhüttenleute / Werkstoffausschuss
oder auch: Bericht des Werkstoffausschusses des Vereins Deutscher Eisenhüttenleute. Nr. 1608.
Versprödung verschiedener Stähle durch Wasserstoffaufnahme aus feuchtem Schwefelwasserstoff
von Verein Deutscher Eisenhüttenleute / Werkstoffausschuss, Erich E. Hofmann
Bei der Korrosion an der Luft, d.h. bei dem bekannten Rosten, reagieren Elektronen aus dem metallischen Eisen (Fe) mit Sauerstoff (O2) und führen unter Beteiligung von Wasser (H2O) zu Hydroxydionen (HO-). Diese bilden mit dem freigesetzten zweiwertigen Eisen (Fe2+) unter weiterer Mitwirkung von Sauerstoff Rost, ein kompliziert aufgebautes wasserhaltiges Oxid des dreiwertigen Eisens. Soweit bekannt, handelt es sich um einen rein chemischen Vorgang.
Im Gegensatz dazu wirken bei der Korrosion unter Ausschluß von Luft die Desulfurikanten mit, die wie in Ursachen beschrieben ohne Sauerstoff leben. Deshalb spricht man von anaerober Biokorrosion. Auf eine noch nicht in allen Details geklärte Weise dienen die Elektronen aus dem Eisen zur Reduktion von Sulfat zu Schwefelwasserstoff (H2S), was den Bakterien die für Ihr Wachstum benötigte Energie liefert.
Der eine Korrosionsmechanismus ist offensichtlich: Diese Bakterien leben davon, daß sie, wie der Name sagt, das harmlose, in natürlichen Wässern häufige Sulfat (in ungelöster Form z.B. als Gips bekannt) zu Schwefelwasserstoff reduzieren. Als Reduktionsmittel für die Umwandlung von Sulfat in Schwefelwasserstoff dienen diesen Bakterien Produkte aus natürlichen Verwesungsprozessen, z.B. im häuslichen Abwässer, die dabei zu Kohlendioxid oxidiert werden. Der Schwefelwasserstoff greift dann das Eisen an, wobei sich pechschwarze Reaktionsprodukte bilden.
Der andere Korrosionsmechanismus ist weniger klar, obwohl schon um 1930 Modellvorstellungen dazu entwickelt wurden. Sulfatreduzierende Bakterien verwenden nämlich auch Wasserstoffgas, um Sulfat zu reduzieren. Weil sich auf Eisen in Wasser langsam Wasserstoffgas, oft als "kathodischer Wasserstoff" bezeichnet, als Produkt bildet, wurde lange angenommen, dass dessen Verbrauch durch die sulfatreduzierenden Bakterien die Auflösung des Metalls im Wasser beschleunigt. Ein solches Prinzip ist aus der Chemie wohlbekannt: Wird das Produkt aus einer antriebsschwachen chemischen Reaktion in einer zweiten, sich anschließenden Reaktion gleich weiter verbraucht, kommt die erste Reaktion auf Touren. Im Falle der Biokorrosion von Eisen ist jedoch diese verlockende Vorstellung offensichtlich nicht haltbar. Am Max-Planck-Institut für marine Mikrobiologie, Bremen, wurden in Zusammenarbeit mit der Amtlichen Materialprüfungsanstalt Bremen und dem Max-Planck-Institut für Eisenforschung, Düsseldorf, Bakterien entdeckt, welche Eisen deutlich schneller korrodieren, als es durch Verbrauch von Wasserstoffgas jemals möglich wäre. Alles spricht dafür, dass sie im engen Kontakt mit dem Eisen diesem direkt Elektronen entziehen und so gewissermaßen den Umweg über "kathodischen Wasserstoff" umgehen. Und Elektronenentzug aus Eisen bedeutet Korrosion. Wie ein Elektronenfluß über die winzig kurze, aber dennoch über eine "Stromleitung" zu überbrückende Strecke zwischen Eisen und Bakterienzellen zustande kommt, ist noch unbekannt. Versteht man erst einmal deren Biochemie, wird man auch gezielter forschen können, um Schutzmaßnahmen zu entwickeln.
Schwefelwasserstoff wird mit dem Methan im Motor verbrannt. Aus H2S und Sauerstoff entsteht bei der Verbrennung ein Stoff (= SO2), der ebenfalls gasförmig ist, sich gut löst und eine sehr saure und korrosive Wirkung hat. Durch dieses Gas versäuert das Motoröl und zerstört dessen Wirksamkeit. In sehr kurzer Zeit kann dadurch der Verbrennungsmotor zerstört werden.
|
(2) |
2H2S + 3O2 |
——► |
2H2O + 2SO2 |
Verbrennung |
|
(3) |
SO2 + H2O |
——► |
H2SO3 |
(=schweflige Säure) Lösen |
Eine weitere chemische Reaktion tritt ein, wenn durch unvollkommener oder gezielt geringer Sauerstoffzufuhr aus H2S elementarer Schwefel entsteht. Dieses Verfahren wird häufig fälschlicherweise zur H2S Elimination benutzt. Die untenstehende Formel zeigt auf, welche korrosiven Nebenwirkungen dabei entstehen.
|
(4) |
2 H2S + O2 |
——► |
2 H2O + 2S |
|
|
|
|
|
|
(5) |
S + H2O + O2 |
Thiobacillen mit S als Substrat ——► |
H2SO4 |
Korrosion zementgebundener Baustoffe
Die so entstehende biogene Schwefelsäure und die vorgenannte schweflige Säure bewirken bei Konzentrationen von > 0,5 ppm H2S Abtragungsraten des Betons von 0,5 mm bis 10 mm pro Jahr. Bei extremen Bedingungen sind schon 20 mm Abtragung festgestellt worden. Das nebenstehende Bild zeigt die Korrosion nach 30 Monaten mit 2-4 ppm H2S und nach 22 Monaten mit 15-25 ppm H2S.
| 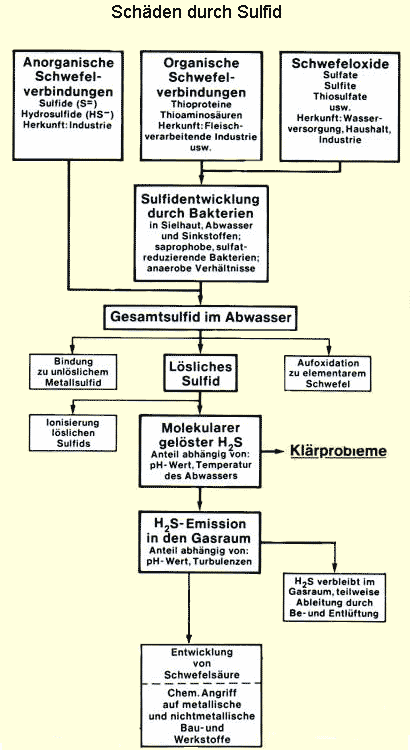
Bildquelle: www.ib-rauch.de |